Курсовая работа: Рефрактометрический метод в экспресс-анализе лекарственных форм. Рефрактометрические методы определения сахаров
Для приготовления водок, кремов, ликеров и бесцветных сладких напитков применяется рафинированный сахар-песок или сахар-рафинад, для остальных напитков - сахар-песок.
Сахар-рафинад представляет собой дополнительно очищенный рафинированный сахар в виде кусков или кристаллов.
Органолептические показатели:
Вкус - сладкий, без посторонних привкуса и запаха;
Цвет - белый с блеском;
Растворимость в воде - полная, раствор должен быть прозрачным, без каких-либо нерастворимых осадков, механических или других посторонних примесей;
Сыпучесть - сыпучий, без комков.
По физико-химическим и органолептическим показателям сахар-рафинад должен соответствовать требованиям, указанным в таблице 3.1.
Таблица 3.1 Физико-химические показатели сахара-песка и сахара-рафинада
При проведении лабораторной работы подгруппа делится на две бригады, каждая из которых анализирует разные образцы сахара-песка или сахара-рафинада.
Задание 1.1 Определить органолептические показатели
Органолептический анализ включает оценку внешнего вида, привкуса, запаха и чистоты раствора сахара.
Внешний вид должен соответствовать требованиям ГОСТ 21 «Сахар-песок. Технические условия» и ГОСТ 22 «Сахар-рафинад. Технические условия».
1.1.1 Определение внешнего вида
Пробу сахара рассыпают на лист белой бумаги толщиной слоя не более 1 см и при рассеянном дневном свете или лампы дневного света визуально определяют внешний вид.
1.1.2 Определение запаха и привкуса
Для определения запаха и привкуса сахара готовят водный раствор, содержащий 25 г сахара в 100 см дистиллированной воды. Раствор сахара помещают в чистую стеклянную банку с пришлифованной пробкой, заполняя ее на 3/4 объема, банку с раствором закрывают пробкой и выдерживают в течение 1 ч при комнатной температуре.
Определение запаха производят на уровне края банки тотчас после открывания пробки. Привкус определяют как в сухом сахаре, так и в его водном растворе.
Задание 1.2 Определить массовую долю влаги
Метод основан на высушивании взвешенной пробы сахара и определении потери массы при высушивании.
Проведение анализа
Навеску сахара-песка или быстро измельченного сахара-рафинада массой (10,000±0,001) г отбирают от средней пробы и помещают в высушенную до постоянной массы бюкс с пришлифованной крышкой.
Высушивают в сушильном шкафу до постоянной массы.
Массовую долю влаги в процентах вычисляют по формуле (3.1):
W = (m 1 – m 2)·100/ m 1 , (3.1)
где m 1 – масса навески до высушивания;
m 2 - масса навески после высушивания.
Задание 1.3 Определить массовую долю сахарозы поляриметрическим методом
Поляриметрический метод определения сахарозы основан на способности углеводов вращать плоскость поляризации луча света. Известно, что колебания обыкновенного светового луча происходят во всех плоскостях, перпендикулярных его направлению.
При прохождении обыкновенного луча света через некоторые кристаллы их решетки способны пропускать лучи только определенного направления колебания. По выходе из кристалла колебания луча будут происходить только в одной плоскости, такой луч называется поляризованным.
Поляриметрические исследования ведут с помощью поляриметров. В ликероводочном производстве широкое распространение получил поляриметр СУ-3, общий вид которого представлен на рисунке 1.
Устройство прибора: основными частями прибора являются узел измерительной головки 1 и осветительный узел 2 , соединенные между собой траверсой 3, на которой укреплена камера 4 для поляриметрических трубок. В передней части прибора имеется лупа в оправе 5 для отсчета показание по шкале и зрительная труба 6, которая имеет гильзу 7. С тыльной стороны измерительной головки находится узел нониуса. В нижней части измерительной головки расположена рукоятка 8 кремальерной передачи для перемещения кварцевого клина и связанной с ним шкалы.
Осветительный узел имеет поворотную обойму 9 со стеклянным светофильтром и матовым стеклом и патрон 10 с лампочкой. Траверса крепится к литому основанию.
Шкала поляриметра при определении сахара показывает его процентное содержание. Для отсчета десятых долей служит нониус.
Перед началом работы необходимо установить прибор на нуль. При этом нулевое значение шкалы должно совпадать с нулем нониуса Трубку заполняют исследуемым раствором, помещают в камеру прибора и производят отсчет показаний шкалы и нониуса.
Рисунок 1 Общий вид поляриметра СУ-3
При анализе левовращающих растворов все операции проводят в обратном направлении, в этом случае нуль нониуса расположен левее шкалы.
Поляризационная трубка длиной 200 мм считается нормальной; при поляризации в трубках длиной 100 или 400 мм показания поляриметра в первом случае удваивают, а во втором уменьшают в 2 раза.
Трубку наполняют следующим образом: один конец ее закрывают пришлифованным круглым стеклом и завинчиваю гайкой. Затем, слегка наклонив трубку, заполняют ее испытуемым раствором так, чтобы жидкость выступала над краем трубки при вертикальном положении. Осторожно, срезая жидкость стеклом, закрывают и затем завинчивают трубку. В жидкости не должно оставаться пузырьков воздуха. Протерев стекла, производят измерение угла вращения раствора. Температура поляризуемого раствора должна быть равна 20°С в течение всего периода измерения.
Для каждой пробы производят не менее трех отсчетов по поляриметру и принимают средний. Полученная величина есть угол вращения раствора.
Проведение анализа
Навеску анализируемого сахара (рафинад предварительно измельчают в ступке) массой (25,00±0,01) г количественно переносят в мерную колбу вместимостью 100 см 3 с использованием горячей дистиллированной воды, которой заполняют колбу примерно на 4/5 объема. Раствор перемешивают вращательными движениями и колбу с содержимым помещают на водяную баню с температурой (20±0,1)°С на 30 мин. Затем объем доводят дистиллированной водой до метки, перемешивают раствор и пропускают через бумажный фильтр.
При фильтрации воронку покрывают часовым стеклом во избежание испарения воды и изменения концентрации. Первые порции фильтрата отбрасывают. Все операции проводят тщательно и быстро.
Фильтрат заливают в поляриметрическую трубку длиной 200 мм с кожухом для водяного охлаждения, помещают в камеру сахариметра и подключают к термостату ТС-15, в котором поддерживается температура (20±0,1) °С.
По истечении 15-20 мин, когда температура в поляриметрической трубке станет равной 20 °С, измеряют угол вращения фильтрата. Поляриметрическое определение необходимо проводить при температуре окружающей среды 20°С.
Значение, непосредственно полученное на шкале сахариметра, дает количество сахарозы в процентах к массе взятого сахара. Результат определяют как среднее арифметических трех определений с точностью до одной сотой процента. Массовую долю сахарозы (X, %) в пересчете на сухое вещество вычисляют по формуле (3.2):
X = (P ·100) / (100 –W) (3.2)
где Р - показание сахариметра (среднее арифметическое трех измерений), %;
W - массовая доля влаги в сахаре, %.
За результат анализа принимают среднее арифметическое трех параллельных измерений, допустимое расхождение между которыми не превышает ±0,05%.
Задание 1.4 Приготовить сахарный сироп и определить массовую концентрацию сахара в сахарном сиропе
1.4.1 Приготовление сахарного сиропа заданной концентрации
Сахар-песок и сахар-рафинад используются в производстве водок и ликероводочных изделий в виде сахарных сиропов преимущественно концентрацией 65,8%. Белый сахарный сироп получают двумя способами: холодным и горячим.
Студентам необходимо сделать расчет и приготовить сахарные сиропы по следующим исходным данным:
Приготовить сахарный сироп с массовой концентрацией 65,8% из анализируемого сахара массой 100 г; сравнить расчетный объем полученного сахарного сиропа с фактическим.
Приготовить 250 мл сахарного сиропа с массовой концентрацией 65,8% из анализируемого сахара.
При расчетах необходимо учесть массовую долю влаги в сахаре, а также принять, что 5% воды испаряется при приготовлении сиропа. Плотность 65,8-%-го раствора составляет 1,3212 г/см 3 .
1.4.2 Определение массовой концентрации сахара в сахарном сиропе
Массовую концентрацию сахара в сахарном сиропе определяют рефрактометрическим методом.
Рефрактометры предназначены для определения концентрации веществ по показателю преломления растворов, содержащих эти вещества.
В контроле ликероводочного производства применяют рефрактометры марок: РЛ, РЛ-1 (рефрактометр лабораторный), РПЛ-3 (рефрактометр пищевой лабораторный), УРЛ-1 (универсальный рефрактометр лабораторный).
Устройство приборов: 1 - призмы измерительные; 2 и 3 - окна для проходящего и отраженного света; 4 - источник света; 5 - компенсатор дисперсии; 6 - прорезь; 7 - окуляр; 8 – термометр.
Измерения на приборе следует проводить строго при температуре (20+0,5) °С, наблюдая ее по термометру. В верхней и нижней камерах, где укреплены призмы, имеются каналы, через которые можно пропускать воду с определенной температурой, передаваемую от ультратермостата с температурой 20 °С.

Рисунок 2 Рефрактометры лабораторные марок РПЛ-3 (а) и УРЛ-1 (б):
Если температура измерения отличается от 20 °С, то следует вносить в показания приборов поправку на температуру.
Перед измерением необходимо проверить нуль прибора. Для этого на нижнюю призму наносят каплю дистиллированной воды и закрывают верхнюю призму. С помощью рукоятки перемещают положение окуляра вниз до тех пор, пока в поле зрения не появится граница светотени. Совмещают визирную линию с границей светотени и проводят отсчет по шкале. При правильной установке прибора на нуль граница светотени при 20 °С должна быть совмещена с нулевым делением шкалы сухих веществ, а также с делением n д = 1,33299 шкалы показателей преломления. В случае отклонения от этих значений ключом устанавливают нуль.
Правильность установки прибора проверяют 2-3 раза.
Аналогично проводят на рефрактометре измерения анализируемого раствора.
Измерения концентрации сахарных растворов можно проводить при температуре 10-30 °С и вносить поправки на температуру 20 °С.
Измерив показатель преломления анализируемого сахарного раствора, находят содержание сахара (г/100 см 3) по таблице 8 .
Задание 1.5 Сравнить полученные результаты анализов сахара-песка и сахара-рафинада с нормативными значениями . Сделать выводы
Задание 1.6 Изучить формы журнала приготовления ликеро- водочных изделий ПЛВ №6
Изучить форму и заполнить соответствующие графы журнала ПЛВ №6 «Журнал учета сахара, поступающего для приготовления сахарного сиропа» (форма журнала выдается преподавателем).
Похожая информация.
Рефрактометрия в фармацевтике.
Процесс измерения концентрации различных веществ методом измерения преломления и определения коэффициента преломления получил своё название - рефрактометрия
. Приборы, использующие в своей работе принцип рефрактометрии, называются рефрактометрами. Широкое применение рефрактометры получили в разных промышленностях: для идентификации химических соединений, определения физико-химических параметров, для количественного и структурного анализа. В пищевой промышленности - для измерения содержания спирта в алкогольных продуктах, контроля содержания сахара в сахарном производстве - в общем, для установления качества пищевых продуктов. В фармакологии рефрактометры применяются для определения количества глюкозы в биологических жидкостях и лекарственных средств в растворах. Достоинства рефрактометрических методов химического количественного анализа - быстрота измерений, малый расход вещества и высокая точность.
Задача работы: Рефрактометрический метод как метод анализа лекарственных веществ. Актуальность использования в фармацевтике и, как частное, – в аптеках.
Теоретическая часть.
Показателем преломления (индексом рефракции) называют отношение скорости света в вакууме к скорости света в испытуемом веществе (абсолютный показатель преломления). Показатель преломления зависит от температуры и длины волны света, при которой проводят определение. В растворах показатель преломления зависит также от концентрации вещества и природы растворителя. При этом на практике определяют так называемый относительный показатель преломления (n), который рассчитывается как отношение синуса угла падения луча (α) к синусу угла преломления (β) для двух соприкасающихся сред.
Показатель преломления также равен отношению скоростей распространения света в этих средах
:
В лабораторных условиях обычно определяют так называемый относительный показатель преломления (ПП) вещества по отношению к воздуху. ПП измеряют на рефрактометрах различных систем. Раньше измерение ПП чаще всего производилось с использованием , работающего по принципу полного внутреннего отражения при прохождении светом границы раздела двух сред с различными показателями преломления. В настоящее время в лаборатории всё чаще можно встретить автоматические рефрактометры ATAGO серии RX.
Диапазон измеряемых ПП при измерении в проходящем свете с использованием , – 1.3000 – 1.7000. Если необходимо раздвинуть границы диапазонов, применяют специальные модели с низкики или высокими диапазонами, а также многоволновые рефрактометры Аббе.
Диапазон измеряемых ПП при измерении на автоматических рефрактометрах серии RX – 1.32500 – 1.70000.
Точность измерения показателя преломления должна быть не ниже ±2·10 -4
Величина показателя преломления зависит от природы вещества, длины волны света, температуры, при которой проводится измерение, и концентрации вещества в растворе. Обычно измерение показателя преломления проводится при длине волны света 589,3 нм (линия D спектра натрия). Но в некоторых случаях используются разные длины волн в диапазоне от 450нм до 1550нм. Очень важным условием определения ПП является соблюдение температурного режима. Как правило, определение выполняется при 20 градусах по шкале Цельсия. При температуре свыше 20 градусов - величина ПП уменьшается, при температуре ниже 20 градусов – величина ПП увеличивается.
Поправка на температуру рассчитывается по формуле:
n 1 =n 20 +(20-T)*0,0002
Показатель преломления, измеренный при 20°
С и длине волны света 589,3 нм, обозначается индексом n 20 .
Показатель преломления может быть использован как константа для установления подлинности и чистоты тех лекарственных препаратов, которые по своей природе являются жидкостями. Рефрактометрический метод широко используется в фармацевтическом анализе для количественного определения концентрации веществ в растворе, которую находят по графику зависимости показателя преломления раствора от концентрации. На графике выбирают интервал концентраций, в котором наблюдается линейная зависимость между показателем преломления и концентрацией. Такой способ может использоваться в практике внутриаптечного контроля.
Зависимость показателя преломления от концентрации вещества в процентах выражается формулой:

Где n и n 0 - показатели преломления раствора и растворителя;
С - концентрация вещества в растворе;
F - фактор показателя преломления.
Показатель преломления раствора складывается из показателя преломления растворителя и показателей преломления растворенных веществ.
Значения показателей преломления и факторов для различных концентраций растворов лекарственных веществ приведены в рефрактометрических таблицах, которые имеются в руководстве по внутриаптечному контролю. Использование таблиц значительно упрощает расчёты.
Зависимость показателя преломления водных растворов некоторых веществ от концентрации:

Определение концентрации вещества в растворе.
В рефрактометрии используют два способа расчёта концентрации вещества в растворе по измеренному показателю преломления.
- Расчет концентрации по формуле:

Значение фактора показателя преломления берется из рефрактометрических таблиц.
- Расчет концентрации по рефрактометрическим таблицам.
Измерив показатель преломления, в таблице находят соответствующее ему значение концентрации. Если измеренный показатель преломления в таблице не приведен, проводится интерполирование.
Рефрактометрический метод используется для количественного определения концентрированных растворов.
Концентрированные растворы - это рабочие растворы лекарственных веществ (ЛВ) опредёленной, более высокой концентрации, чем эти растворы прописываются в аптеках.
При приготовлении концентрированных растворов следует избегать концентраций близких к насыщенным, т.к. при понижении температуры раствора возможна кристаллизация растворённого вещества.
Отклонения, допускаемые в концентратах:
при содержании ЛВ до 20% - не более ± 2% от обозначенного процента;
при содержании ЛВ свыше 20% - не более ± 1% от обозначенного процента (Пр. МЗ РФ от 16.10.97).
Формулы расчёта для исправления концентрации растворов, изготовленных массообъёмным способом.
1) Концентрация раствора оказалась выше требуемой.
Объем воды, необходимый для разбавления полученного раствора, вычисляют по формуле:

Где Х - количество воды, необходимое для разбавления изготовленного раствора (мл.);
А - объём изготовленного раствора (мл.);
С - фактическая концентрация раствора (%).
2) Концентрация раствора оказалась ниже требуемой.
Массу ЛВ для укрепления полученного раствора вычисляют по формуле:

Где Х - масса вещества, которую следует добавить к раствору (г);
А - объем изготовленного раствора (мл.);
В - требуемая концентрация раствора (%);
С - фактическая концентрация раствора (%);
ρ
20 - плотность раствора при 20°
С (г/мл, г/см 3)
Рефрактометры, лучше всего подходящие для аптек: , серия NAR/ , ATAGO.
Рефрактометры серии NAR или DR-A1 предназначены для измерения показателя преломления и средней дисперсии неагрессивных жидкостей. Это очень качественный приборы. Простые в обслуживании. Минимальны в содержании. Фактически расходный материал для этих рефрактометров – лампочка (источник света).
Рефрактометры ATAGO
серии или применяются:
1.В медицинских учреждениях для определения белка в моче, сыворотке крови, плотности мочи, анализ мозговой и суставной жидкости, плотности субретинальной и других жидкостей глаза. Использование рефрактометра позволяет значительно сократить затраты времени при массовых обследованиях пациентов.
2.В фармацевтической промышленности рефрактометры ATAGO могут применяться для исследования водных растворов различных лекарственных препаратов: кальция хлорида (0% и 20%); новокаина (0,5%, 1%, 2%, 10%, 20%, 40%); эфедрина (5%); глюкозы (5%, 25%, 40%); магния сульфата (25%); натрия хлорида (10%); кордиамина и т.д.
3.В пищевой промышленности используют рефрактометры ATAGO на сахарных и хлебных заводах, кондитерских фабриках для анализа продуктов и сырья, полуфабрикатов, кулинарных и мучных изделий, для определения влажности меда (до 30 %). В производстве сахара широкое применение получили поляриметры АТАГО. Поляриметры на сахарном заводе измеряют концентрацию и чистоту сахара в сахарной свекле или сахарном тростнике на этапе приемки сырья.
Для определения доли сухих веществ в различных суслах (ГОСТ 5900-73), сахароагаровом сиропе, сиропе для мармелада, зефира, кремов и пряников.
Для определение массовой доли растворимых сухих веществ по сахарозе (% Brix) в продуктах переработки плодов и овощей, для определения процентного содержания жира в твёрдых продуктах питания (пряниках, вафлях или хлебобулочных изделиях) концентрации солей.
4.При обслуживании техники применяются рефрактометры ATAGO для определения с большей точностью объёмной концентрации противокристаллизационной жидкости "ИМ", которая добавляется в авиационное топливо в количестве от 0,1 до 0,3%. Дальнейшая обработка результатов ведется согласно "Методическим рекомендациям по анализу качества ГСМ в гражданской авиации" Ч. II стр.159. Опыт использования рефрактометров показал, что эти приборы значительно сокращают время и повышают достоверность получения анализов по процентному содержанию жидкости "ИМ" в авиационном топливе.
Автоматический лабораторный рефрактометры серии RX с микропроцессорным управлением предназначены для исследования концентрации широкого диапазона жидких сред как низкой, так и высокой вязкости, независимо от прозрачности и цвета. обеспечивают высокую точность измерения, точный контроль за температурой. Весь процесс измерения (нагрев/охлаждение) проходит в автоматическом режиме. Достаточно просто нажать клавишу Старт. Прибор автоматически измеряет коэффициент преломления образца раствора, вычисляет его концентрацию и представляет результат на цифровом ЖК-экране. снабжен экраном, который выполнен по технологии «Тач скрин» - сенсорный экран, всё управление прибором осуществляется с экрана. Автоматические рефрактометры серии RX могут как нагревать/охлаждать образец за счет встроенных элементов Пельтье, так и использовать функцию автоматической температурной компенсации при проведении измерения. Идеальный прибор для фармацевтов из этой серии - автоматический рефрактометр и .
Определение концентрации спирта в лекарственных формах рефрактометрическим методом.
Спирт этиловый (этанол, Spiritus aethylicus) - один из наиболее широко используемых органических растворителей в медицинской и фармацевтической практике. Этанол обладает бактериостатическими и бактерицидными свойствами. Широко используется для получения настоек, экстрактов, лекарственных форм для наружного применения. Качество спиртовых растворов зависит от концентрации спирта, в котором растворён препарат. В каждом случае необходима оптимальная концентрация, при которой лекарственное вещество не выделится в осадок. Поэтому готовятся водно-спиртовые растворы с различной концентрацией спирта. Количественное содержание этилового спирта легко определяется рефрактометрическим методом. Существует чёткая зависимость между концентрацией этилового спирта и коэффициентом преломления. Известно, что показатель преломления зависит от температуры, длины волны света, природы вещества и растворителя, концентрации вещества. Так вот показатель преломления водных растворов спирта от 1% до 70% имеет линейную характеристику, а значит можно легко измерить концентрацию рефрактометром. АТАГО производит специальные рефрактометры для измерения концентрации спирта. В общем, это обыкновенные рефрактометры, но в процессор «вшит» специальный поправочный коэффициент, позволяющий отображать на дисплее сразу же концентрацию водно-спиртового раствора, минуя показатель преломления. При концентрации от 70% до 96% - зависимость нелинейная. Таким образом, рефрактометрическим методом можно определить крепость спирта в пределах от 1% до 70%.
Практическая часть.
Рассмотрим применение рефрактометров при изготовлении и анализе раствора глицерина 10% для инъекций: Раствор глицерина 10% Глицерина (в пересчете на безводный) 100 г
1. Натрия хлорид 9,0 г. Воды до 1л.
Изготовление. От поставщиков покупается глицерин (высший сорт, динамитный) с количественным содержанием 86-90%, 94-98% и более. Поэтому, чтобы рассчитать количество исходного глицерина, необходимо точно знать, какова в нем массовая доля безводного вещества. Для точного измерения концентрации глицерина применяют рефрактометр. Показатель преломления исходного глицерина n=1,4569 соответствует массовой доле безводного вещества 89%. Исходное количество глицерина, которое требуется для изготовления раствора, по прописи 68:
2. Масса глицерина = 100 г./ 0,89 = 112,36 г.
Количественное определение глицерина в растворе. Вычисляем концентрацию глицерина:
С глиц = / F глиц,
где n - показатель преломления раствора;
n 0 - показатель преломления воды очищенной, измеренный при той же температуре;
С NaCl - концентрация натрия хлорида в растворе, определенная методом аргентометрии;
F NaCl - фактор показателя преломления раствора натрия хлорида для найденной концентрации;
F глиц - фактор преломления 10% раствора глицерина (0, 001156).
В фармацевтической промышленности рефрактометры ATAGO могут применяться для исследования водных растворов различных лекарственных препаратов: кальция хлорида (0% и 20%); новокаина (0,5%, 1%, 2%, 10%, 20%, 40%); эфедрина (5%); глюкозы (5%, 25%, 40%); магния сульфата (25%); натрия хлорида (10%); кордиамина и т.д.
Примечание:
Если для одного из веществ, входящих в раствор, фактор показателя преломления неизвестен или незначительная его концентрация не позволяет получить точных данных, то готовят контрольный раствор, содержащий это вещество в той концентрации, которая была определена титрометрическим методом.
нашли применение во всех отраслях промышленности РФ. Рефрактометры и поляриметры АТАГО внесены в госреестр средств измерений РФ. Это позволяет применять приборы АТАГО в самых жёстко контроллируемых сферах производств - таких, как, например, фармацевтика.
Общая характеристика метода
Рефрактометрия - оптический метод исследования, основанный на измерении показателя преломления луча света, проходящего через исследуемое вещество.
В основе метода лежит явление рефракции, то есть преломление световых лучей на границе раздела двух различных по своей природе оптических сред.
Рефракция света является следствием его взаимодействия с частицами вещества, через которое проходит свет. Под воздействием электромагнитных колебаний света в атомах вещества возникают вынужденные колебания электронов и ядер. Вследствие этого происходит их смещение относительно друг друга, что приводит к несовпадению «центров тяжести» отрицательного и положительного электричества в атомах и молекулах, то есть атомы, и молекулы вещества поляризуются в электромагнитном поле света.
Преломление света оценивается показателем преломления n, который равен отношению синуса угла падения? к синусу угла преломления?:
Показатель преломления зависит от ряда факторов: природы вещества, длины волны падающего света, плотности среды, концентрации раствора и температуры. Существует прямолинейная зависимость между величиной показателя преломления и концентрацией сахара в водном растворе, которая используется при определении концентрации сахара в растворах.
Метод рефрактометрии применяется также для идентификации веществ, определения их чистоты и концентрации в растворе.
Зависимость показателя преломления от плотности вещества выражается формулой:
где n - показатель преломления;
r - удельная рефракция вещества, см3/г;
d - плотность вещества, г/см3.
Функция f(n) выражается соотношением:
Размерность удельной рефракции соответствует удельному объему, то есть r, см3/г.
Умножение удельной рефракции r на молярную массу вещества МВ дает величину молярной рефракции RM:
Подставив значение удельной рефракции r в формулу (2.19), получают уравнение, связывающее молярную рефракцию вещества с его плотностью, молярной массой и поляризуемостью:
где RM - молярная рефракция вещества В см3/моль;
МВ - молярная масса вещества В, г/моль;
n - показатель преломления вещества В;
d - плотность вещества В, г/см3.
Выражение (2.20) носит название формулы Лорентц - Лоренца. Она при меняется в расчетах и достаточно точно отвечает правилу аддитивности молекулярной рефракции. Рассчитанные по этой формуле результаты мало зависят от изменений температуры, давления и агрегатного состояния вещества во время анализа.
Правило аддитивности молекулярной рефракции заключается в следующем: сумма атомных рефракций элементов, входящих в соединение, равна молекулярной рефракции этого соединения.
где? - коэффициент поляризуемости, см3;
NA - постоянная Авогадро, 6,02204 1023 моль-1.
Коэффициент поляризуемости (?) зависит от объема атомов и молекул вещества и не зависит от температуры. Экспериментально установлено, что? ? r3, где r - радиус поляризованной молекулы.
Физический смысл молярной рефракции поясняет соотношение:
где NA - число молекул в 1 моль вещества, моль-1;
Объем шара, т.е. объем поляризованной молекулы;
Отсюда следует, что RM - суммарный объем всех поляризованных молекул, содержащихся в 1 моль вещества. Объем поляризованных молекул состоит из объемов атомов и объемов, занимаемых двойными и тройными связями. Объем атомов называют атомной рефракцией Rат, а объем связи - рефракцией связи Rсв. Из сказанного видно, что молярная рефракция - аддитивная величина.
Значения рефракций атомов некоторых элементов и связей представлены в таблице 2.8
Таблица 2.8- Атомные рефракции и рефракции связей по Фогелю
Сущность определения содержания сахара в сухих винах с использованием колоночной хроматографии методом рефрактометрии
Рефрактометрическое определение содержания сахара в пищевых продуктах основано на существовании прямолинейной зависимости между величиной показателя преломления и концентрацией сахара в растворе.
Оборудование
1. Рефрактометр ИРФ - 454 БМ;
2. Аналитические весы;
3. Мерные колбы объемом 25 см3 (5 шт.);
4. Пипетка глазная;
5. Хроматографическая колонка;
6. Фильтровальная бумага.
Применяемые реактивы
1. Водно - спиртовый раствор. Приготовление ведется с учетом содержания спирта. Например, на этикетке указано «Алк. 9 - 11% об.», следовательно, водно - спиртовый раствор готовится в соотношении 91:9 частей;
2. Дистиллированная вода;
Измерение показателя преломления исследуемых веществ проводят на рефрактометре ИРФ - 454БМ, принцип действия которого основан на явлении полного внутреннего отражения при прохождении светом границы раздела двух сред с разными показателями преломления. Все измерения проводят в «белом свете» (дневном или электрическом). Для получения высокой точности показатели преломления исследуемых жидкостей замеряют при определенной температуре и определенной длине волны.

Рисунок 2.14 - Рефрактометр ИРФ - 454БМ: 1 - окуляр; 2 - маховики; 3, 4 - зеркала; 5 - рефрактометрический блок с подвижной (а) и неподвижной (б) призмами; 6 - заслонка; 7 - крючок; 8 - корпус прибора; 9 - место установки термометра

Рисунок 2.15 - Схема призм рефрактометра: 1 - измерительная призма; 2 - исследуемая жидкость; 3 - осветительная призма
Порядок работы рефрактометра ИРФ - 454БМ
Рефрактометр устанавливают так, чтобы свет падал на входное окно осветительной призмы и на зеркало, которым направляют свет во входное окно измерительной призмы. Для этого нужно открыть заслонку 6 и зеркала 3, 4 (см. рисунок 2.14).
Осветительную призму открыть на угол 100°. На чистую полированную поверхность измерительной призмы 1 (см. рисунок 2.15) стеклянной палочкой или пипеткой, не касаясь призмы, нанести 2 - 3 капли жидкости так, чтобы вся поверхность была покрыта пленкой жидкости. Опустить осветительную призму 3 и прижать ее крючком 7. Измерения прозрачных жидкостей проводят в проходящем свете, когда он проходит через открытое окно осветительной призмы.
Лучи света проходят осветительную призму 3, рассеиваясь на выходе матовой гранью А1В1, входят в исследуемую жидкость и падают на полированную грань АВ измерительной призмы 1 (см. рисунок 2.15). Поворотом зеркала 3 (см. рисунок 2.14) ярко освещают призму белым светом. Все поле в окуляре должно быть освещено равномерно.
Наличие темных пятен указывает на недостаточное количество взятой для анализа жидкости. В таком случае призмы раскрывают и добавляют несколько капель исследуемой жидкости и снова плотно сжимают их.
До начала измерений проверьте чистоту осветительной и измерительной призм прибора (смочите их дистиллированной водой и протрите чистой мягкой салфеткой).
Перед измерениями проверяют рефрактометр по дистиллированной воде:
а) на чистую полированную поверхность измерительной призмы осторожно, не касаясь ее поверхности, наносят пипеткой 2 - 3 капли дистиллированной воды и опускают осветительную призму;
б) поворотом зеркала добиваются наилучшей освещенности шкалы. Вращением нижнего маховика, расположенного на правой стороне рефрактометра и смотря в окуляр, границу светотени вводят в поле зрения окуляра 1. Вращением верхнего маховика устраняют цветную окраску границы раздела света и тени и наводят ее на резкость;
в) наблюдая в окуляр, совмещают центр перекрестия с линией светотени с помощью нижнего маховика и измеряют значение показателя преломления воды на шкале, расположенной внизу окуляра.
При 20°С показатель преломления воды nD = 1,3330. Если опыт проводился при другой температуре (измерить температуру воды термометром), то вводится температурная поправка к полученному значению показателя преломления для воды:
N = 0,0565 10-4 + 10-4 (t0 - 10) (2.23)
где 10-4 - температурный коэффициент показателя преломления дистиллированной воды, 1/град.
n = n?D + ?n (2.24)
Совпадение экспериментально полученного значения n с данными таблицы 2.9 при той же температуре говорит о том, что рефрактометр настроен.
Таблица 2.9 Температурные отклонения показателя преломления воды
Выполнение работы
1) Приготовить растворы для построения градуировочного графика
Готовят пять градуировочных растворов сахарозы в мерных колбах емкостью 25 см3, охватывая диапазон ожидаемой концентрации в исследуемом образце (например, на этикетке вина написано: «сахара 30 - 50 г/дм3», следовательно, нужно приготовить растворы сахара концентрации 20; 30; 40; 50; 60 г/дм3). В качестве растворителя используют водно - спиртовый раствор.
Градуировочные растворы готовятся из массы навески сахарозы при приготовлении 25 см3 раствора с концентрацией сахара 20 г/дм3 по соотношению:
20 г - 1000 см3.
m1, г - 25 см3.
Навеску сахарозы количественно переносят через воронку в мерную колбу вместимостью 25 см3. В колбу добавляют водно - спиртовой раствор на? ее объема и перемешивают содержимое до полного растворения сахарозы. Затем оставшийся объем довести до метки водно - спиртовым раствором и перемешивают. Аналогично рассчитывают и готовят растворы других концентраций.
2) Измерить показатель преломления градуировочных растворов:
а) приподнять осветительную призму и поверхности обеих призм осторожно протереть фильтровальной бумагой;
б) нанести 2 капли раствора на поверхность измерительной призмы и опустить осветительную призму;
в) поворотом верхнего маховика установить границу светлого и темного полей. Она должна быть четкой и не иметь радужной окраски;
г) вращать нижний маховик до совпадения границы темного и светлого участка поля зрения.
д) полученные данные занести в таблицу 2.10;
Таблица 2.10 - Результаты эксперимента
3) Подготовить исследуемый продукт к анализу. Вино, полученное для анализа предварительно пропускают через хроматографическую колонку, заполненную активированным углем, чтобы отделить красящие органические вещества. Устанавливают скорость капания, равную вытеканию 1 капли через каждые 3 с. Если вино недостаточно осветлилось, операцию повторяют 2 - 3 раза.
4) Измерения показателя преломления очищенного вина ведется аналогично измерению показателя преломления градуировочных растворов.
5) По окончании измерений промыть обе призмы дистиллированной водой и вытереть насухо фильтровальной бумагой.
6) Построить градуировочный график по результатам таблицы 2.10.
7) Используя градуировочный график, определите содержание сахарозы в вине, и сравнить с данными на этикетке бутылки.
Обработка результатов эксперимента
1) Проверяют рефрактометр по дистиллированной воде
Показатель преломления по дистиллированной воде n = 1,3302 при температуре проведения эксперимента Т = 28,8°С
N = 0,0565 10-4 + 1 10-4(t - 10) = 0,0565 10-4 + 1 10-4(28,8 - 10) = 1,89 · 10-3
n = n?D + ?n = 1,3302 + 1,89 · 10-3 = 1,33209 ~ 1,3321
2) Построить градуировочный график по результатам таблицы 2.11
Таблица 2.11- Результаты эксперимента

Рисунок 2.16 - График зависимости показателя преломления n от концентрации водно - спиртового раствора сахарозы, г/дм3
3) Используя градуировочный график, определить содержание сахарозы в вине, и сравнить с данными на этикетке бутылки.
Показатель преломления для образца вина n = 1,3390
Уравнение прямолинейной зависимости показателя преломления n от концентрации водно - спиртового раствора сахарозы, г/дм3: n = 1,34426 · 10?4 · C + 1,33425, следовательно:
n = 1,34426 · 10?4 · C + 1,33425
1,3390 = 1,34426 · 10?4 · C + 1,33425
0,00475 = 1,34426 · 10?4 · C
C = 35,3354 ~ 35,33 г/дм3
Анализируемое винное изделие - полусладкое белое столовое вино «Русская Лоза Мускат», алк 10 - 12%, сахар 30 - 40% объем 0,7л
Область применения
1) Круговорот углекислого газа в природе
Углеводы образуются в растениях в процессе фотосинтеза из поглощаемого диоксида углерода атмосферы и воды.
2) Источник пищи
Углеводы служат основным ингредиентом пищи млекопитающих. Общеизвестный их представитель - глюкоза - содержится в растительных соках, плодах, фруктах и особенно в винограде (отсюда ее название - виноградный сахар). Она является обязательным компонентом крови и тканей животных и непосредственным источником энергии для клеточных реакций. Приём пищи увеличивает расход энергии в покое в среднем до 2200 ккал (белки до 30%, углеводы и жиры на 4 - 15%). Эта способность пищи повышать энерготраты называется специфически - динамическим действием пищи.
3) Энергетическая и строительная функция углеводов
Углеводы входят в состав клеток и тканей всех растительных и животных организмов. Они имеют большое значение как источники энергии в метаболических процессах. Для жизнедеятельности организма необходима энергия. Она освобождается в процессе диссимиляции сложных органических соединений: белков, жиров и углеводов, потенциальная энергия которых при этом переходит в кинетические виды энергии, в основном в тепловую, механическую и частично в электрическую.
Расщепление идет путем присоединения кислорода - окисления. При окислении 1 г жира в организме выделяется 9,3 ккал тепла, 1 г углеводов - 4,1 ккал, 1 г белка - 4,1 ккал.
То количество тепла, которое выделяется при окислении в организме 1 г вещества, называется теплотой сгорания.
Часть освободившейся энергии используется для построения новых клеток и тканей, часть потребляется в процессе функционирования органов и тканей - сокращения мышц, проведения нервных импульсов, синтеза ферментов и гормонов и др. Большая часть химической энергии переходит в тепло, которое идет на поддержание постоянной температуры тела.
4) Строительный материал
Целлюлоза является распространенным растительным полисахаридом, входит в состав древесины, скелета стеблей и листьев, оболочки зерновых культур, овощей и фруктов.
5) Кулинарное и кондитерское дело
Химически подтверждают: температура выше 120°С разрушает питательные вещества и запускает реакции, в результате которых образуются элементы, способные навредить организму. Так, готовка на открытом огне вызывает реакцию Майяра: этот французский химик обнаружил, что высокая температура меняет качество аминокислоты в присутствии сахара.
Именно эта реакция придает характерный цвет хлебной корочке, куриной коже, чипсам. Кроме того, благодаря ей появляется аппетитный запах жаренного.
6) Постоянство внутреннего состава крови
Для человека основным источником углеводов является растительная пища. В пище содержатся главным образом сложные углеводы: полисахариды - крахмал, гликоген и дисахариды - молочный, свекловичный, тростниковый и другие сахара. В пищеварительном тракте при их расщеплении образуются простые моносахариды - глюкоза, фруктоза и галактоза, которые всасываются из кишечника в кровь.
В крови углеводы содержатся в виде глюкозы 4,44 - 6,66 ммоль/л, в печени и мышцах - в виде небольших запасов гликогена.
При голодании запасы гликогена уменьшаются, так как гликоген расщепляется до глюкозы и поступает в кровь, поддерживая постоянный уровень сахара в крови. Состояние, когда уровень сахара в крови становится ниже 4,44 ммоль/л, называют гипогликемией, повышение свыше 6,66 ммоль/л - гипергликемией. При гликемии нарушается функциональное состояние нервных клеток, у человека появляются слабость, чувство голода, понижается работоспособность.
Если гипогликемия продолжается длительное время, то человек теряет сознание и может наступить смерть. В случаях, когда человек принимает одномоментно 150 - 200 г легкоусвояемых углеводов (сахар, конфеты), возникает так называемая алиментарная (пищевая) гипергликемия, которая сопровождается глюкозурией - появлением сахара в моче; избыток сахара выводится почками. Всосавшиеся в кишечнике моносахариды с током крови через портальную вену попадают в печень, где часть их превращается в гликоген и откладывается про запас.
Кроме, печени гликоген откладывается в скелетных мышцах. Всего в запасе организма имеется около 350 г гликогена.
7) Применение в медицине для получения антибиотиков
Стрептомицин - антибиотик группы аминогликозидов широкого спектра действия - основание, растворим в воде, термоустойчив. Обладает устойчивостью как в сухом состоянии, так и в растворах (в особенности при рН = 3 - 7 и температуре раствора < 28°С). Обычно выделяют в виде солей: хлоргидрат, сульфат и др.; [?]D26 водного раствора хлоргидрата - 86,1°.
Исторически первый антибиотик группы аминогликозидов и первый, оказавшийся активным против туберкулёза и чумы. Был открыт вторым после пенициллина Зельманом Ваксманом, за что он получил Нобелевскую премию в 1952 году.

стрептомицин
Образуется в процессе жизнедеятельности лучистых грибов Streptomyces globisporus streptomycini или других родственных микроорганизмов.
После введения стрептомицин быстро и полностью всасывается из места инъекции.
Распределяется во всех тканях организма. Связывание с белками плазмы низкое (0 - 10%). Не метаболизируется. T1/2 - 2 - 4 ч. Выводится в неизмененном виде с мочой.
8) Информационная функция
Нуклеиновые кислоты или полинуклеотиды - это сополимеры четырех типов нуклеотидов, представляющих собой сложные эфиры фосфорной кислоты и пентозы (пятичленного циклического сахара), в молекуле которой одна из гидроксильных групп замещена азотистым основанием.
В природе существует два типа нуклеиновых кислот, различающихся входящими в их молекулы пентозами - рибонуклеиновая кислота (РНК), содержащая рибозу, и дезоксирибонуклеиновая кислота (ДНК), содержащая дезоксирибозу.
Дезоксирибонуклеиновая кислота (ДНК) - макромолекула, обеспечивающая хранение, передачу из поколения в поколение и реализацию генетической программы развития и функционирования живых организмов. ДНК содержит информацию о структуре различных видов РНК и белков.
Так же, как ДНК, рибонуклеиновая кислота (РНК) состоит из длинной цепи, в которой каждое звено называется нуклеотидом.
Каждый нуклеотид состоит из азотистого основания, сахара рибозы и фосфатной группы. Последовательность нуклеотидов позволяет РНК кодировать генетическую информацию.
Все клеточные организмы используют РНК для программирования синтеза белков.
В нашей теории показателя преломления имеется еще одно предсказание, которое можно проверить экспериментально. Предположим, что мы рассматриваем смесь двух материалов. Показатель преломления смеси не будет средним двух показателей, а определяется через сумму двух поляризуемостей, как в уравнении (32.34). Если, скажем, мы интересуемся показателем преломления раствора сахара, то полная поляризуемость будет суммой поляризуемостей воды и сахара. Но каждая из них, разумеется, должна подсчитываться исходя из данных о числе молекул данного сорта в единице объема. Другими словами, если в данном растворе содержится молекул воды, поляризуемость которой , и молекул сахарозы , поляризуемость которой , то мы должны получить
 . (32.37)
. (32.37)
Этой формулой можно воспользоваться для экспериментальной проверки нашей теории - измерения показателя для различных концентраций сахарозы в воде. Однако здесь мы должны сделать несколько допущений. Наша формула предполагает, что при растворении сахарозы никакой химической реакции не происходит и что возмущение индивидуальных осцилляторов при различных частотах отличается не слишком сильно. Поэтому наш результат, безусловно, будет только приближенным. Тем не менее давайте посмотрим, насколько он хорош.
Раствор сахара мы выбрали потому, что мы располагаем хорошими данными измерений показателя преломления и, кроме того, сахар представляет собой молекулярный кристалл и переходит в раствор без ионизации и других изменений химического состояния.
В первых трех столбцах табл. 32.2 приведены данные из указанного справочника. В столбце А дан процент сахарозы по весу, в столбце В приведена измеренная плотность в , а в столбце С даны измерения показателя преломления света с длиной волны 589,3 ммк. В качестве показателя чистого сахара мы взяли результаты измерений для кристалла сахара. Эти кристаллы не изотропны, так что показатель преломления в разных направлениях различен. Справочник дает три величины:
Мы взяли среднее.
|
Весовая доля сахарозы |
Плотность, |
Молей сахарозы в литре |
Молей воды в литре |
|||||
|
Чистая вода. Кристаллы сахара. Среднее (см. текст). Молекулярный вес сахарозы. Молекулярный вес воды.., приведенную в столбце I. Из нашей теории мы ожидали, что все величины должны получиться одинаковыми. Они получились хотя и не точно равными, но довольно близкими друг к другу. Отсюда можно заключить, что наши идеи правильны. Более того, мы нашли, что поляризуемость молекул сахара, по-видимому, не зависит сильно от ее окружения: их поляризуемость приблизительно одна и та же как в разбавленном растворе, так и в кристалле. | ||||||||
Цель работы : изучение зависимости показателя преломления раствора сахара от его концентрации.
Принадлежности : рефрактометр ИРФ – 22, набор растворов различной концентрации.
Контрольные вопросы
1. Законы отражения света.
2. Законы преломления света. Показатель преломления.
3. Полное отражение. Предельный угол полного отражения.
4. Ход лучей в треугольной призме. Световоды.
Выполнение работы
Рефрактометр используется для быстрого определения показателя преломления жидкостей, взятых в небольших количествах, показатель преломления которых лежит в пределах 1,3 – 1,7.
Оптическая схема интерферометра приведена на рисунке 1.
Свет, отразившись от зеркала 1, проходит осветительную призму 2, тонкий слой жидкости и измерительную призму 3. Затем через защитное стекло 4 и компенсатор дисперсии 5 попадает в объектив 6, проходит через призму полного отражения 7, пластинку с перекрестьем 8 и через окуляр зрительной трубы 9 попадает в глаз наблюдателя. Шкала прибора освещается с помощью зеркала и проецируется системой призм в фокальной плоскости окуляра, так, что в поле зрения одновременно видны граница света и тени, перекрестье и шкала. Для нахождения границы раздела света и тени и совмещения ее с перекрестьем измерительную головку можно вращать вокруг горизонтальной оси с помощью винта, находящегося на лицевой панели прибора.
1. Расположить осветитель так, чтобы свет падал на зеркало подсветки шкалы и на грань осветительной призмы. Вращая окуляр, фокусируют шкалу и визирное перекрестье.
2. Отвести вверх верхнюю часть измерительной головки с осветительной призмой и нанести на полированную грань измерительной призмы 2 – 3 капли дистиллированной воды. После этого ставят осветительную призму на место. Исследуемая жидкость должна занимать весь зазор между гранями призм.
3. Вращая ручку поворота измерительной головки, добиваются появления в поле зрения границы светлого и темного полей. Окраска границы раздела устраняется компенсатором.
4. Совместить границу раздела с перекрестьем и записать соответствующие этой наводке отсчеты по шкале концентраций и показателя преломления.
5. Затем производят измерения концентрации и показателя преломления всех растворов известной концентрации и построить график зависимости показателя преломления от концентрации сахара.
6. Определить показатель преломления раствора неизвестной концентрации и по графику определить его концентрацию.
Решить задачи.
1. Луч света выходит из скипидара в воздух. Предельный угол полного отражения для этого луча равен . Определить показатель преломления скипидара.
2. Человек с лодки рассматривает предмет, лежащий на дне водоема. Определить его глубину, если при определении «на глаз» по вертикальному направлению глубина водоема кажется равной 1,5 м.
3. Предельный угол полного отражения на границе стекло – жидкость равен . Определить показатель преломления жидкости, если показатель преломления стекла равен 1,5.
РАБОТА 9
ОПРЕДЕЛЕНИЕ ПОСТОЯННОЙ СТЕФАНА-БОЛЬЦМАНА И ПОСТОЯННОЙ ПЛАНКА
Цель работы : знакомство с оптическими методами измерения температуры и определение постоянной Стефана – Больцмана и постоянной Планка.
Принадлежности : пирометр с исчезающей нитью, источник тока, лампа накаливания, регулятор напряжения однофазный.
Контрольные вопросы
1. Что называется тепловым излучением? Его свойства.
2. Что называется потоком излучения?
3. Что такое энергетическая светимость?
4. Что такое абсолютно черное тело?
5. Правило Прево. Закон Кирхгофа.
6. Закон Стефана – Больцмана.
7. Закон смещения Вина.
8. Формула Планка.
9. Оптическая пирометрия.
Введение
В настоящей работе определяется яркостная температура. Для этой цели используется пирометр с исчезающей нитью. Принципиальная схема прибора изображена на рисунке 1. С помощью объектива 5 изображение светящейся поверхности исследуемого тела совмещается с плоскостью нити накала фотометрической лампы 4. Нить и изображение тела рассматриваются через окуляр 1 и светофильтр 3, пропускающий свет с длиной волны = 660 нм.
 Яркость нити можно регулировать путем изменения идущего по ней тока с помощью реостата, рачка которого выведена в виде кольца 2 вокруг окуляра.
Яркость нити можно регулировать путем изменения идущего по ней тока с помощью реостата, рачка которого выведена в виде кольца 2 вокруг окуляра.
При измерениях ток через нить подбирается так, чтобы она не была видно на фоне поверхности исследуемого тела, т.е. чтобы спектральные плотности излучательности нити и исследуемого тела были равны для монохроматического света с длиной волны .
Шкала амперметра пирометра предварительно градуируется по излучению абсолютно черного тела. Поэтому с помощью такого пирометра можно определить яркостную температуру тела.
Если излучение происходит в среде, температура которой , то поток энергии, излучаемой телом в единицу времени вследствие излучения, будет равен
![]() , 1.9
, 1.9
где Т – температура тела, S – площадь его поверхности.
В качестве теплового излучателя в данной работе берется вольфрамовая нить лампочки накаливания, нагреваемая электрическим током. Для поддержания температуры нити постоянной к ней подводится мощность . Часть этой мощности отводится в виде тепла, вследствие теплопроводности среды, а остальная компенсирует излучаемую мощность. И поэтому мы можем записать
![]() , 2.9
, 2.9
где - коэффициент, учитывающий потери энергии на теплопроводность. Приравнивая правые части выражений 1.9 и 2.9 можно получить:
![]() , 3 .9
, 3 .9
где U – напряжение на лампе, I – сила тока в ней, Т – температура нити, измеренная пирометром (яркостная температура).
В данной задаче, как показывает опыт, можно считать, что и тогда из выражения 3.9 можно найти
 , 4.9
, 4.9
где Т – яркостная температура,
Комнатная температура,
S – площадь нити накаливания лампы,
U и I – напряжение на лампе и сила тока в ней.
Зная постоянную Стефана – Больцмана и постоянную Больцмана можно определить постоянную Планка
 , 5.9
, 5.9
где - скорость света в вакууме,
![]() - постоянная Больцмана.
- постоянная Больцмана.
Выполнение работы.
Включить установку в сеть и подать на лампу напряжение 60 – 80 В.
Сфокусировать изображение нити накала фотометрической лампы. Убедиться в том, что изображение нити фотометрической лампы накладывается на изображение нити накаливания исследуемой лампы.
Нажав кнопку К и вращая кольцо пирометра подобрать ток в фотометрической лампе так, чтобы ее изображение исчезало бы на фоне нити исследуемой лампы.
По шкале пирометра определить яркостную температуру нити накаливания лампы. Результаты измерений занести в таблицу 1.
2. Поток излучения абсолютно черного тела равен 10 кВт, максимум спектральной плотности энергетической светимости приходится на длину волны равную 0,8 мкм. Определить площадь излучающей поверхности.
3. Определить коэффициент серости тела, для которого температура, измеренная радиационным пирометром равна 1400 К, тогда как истинная температура тела равна 3200 К.
Работа 1. Определение фокусного расстояния и оптической силы
собирающей и рассеивающей линз ……………………………. 1
Работа 2. Интерференция света ……………………………………………… 4
Работа 3. Дифракция света……………………………………………………. 7
Работа 4. Дифракционная решетка…………………………………………… 11
Работа 5. Изучение фотоэффекта …………………………………………….. 13
Работа 6. Определение длины световой волны с помощью дифракционной
решетки……………………………………………………………… 16
Работа 7. Проверка закона Малюса…………………………………………… 19
Работа 8. Определение показателя преломления раствора сахара
и его концентрации в растворе с помощью рефрактометра ИРФ - 22… 20
Работа 9. Определение постоянной Стефана – Больцмана и постоянной
Планка……………………………………………………………….. 22
 Ударение в английском языке
Ударение в английском языке 10 слов с ударением на 1 слог
10 слов с ударением на 1 слог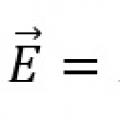 Закон Ома для замкнутой цепи и неоднородного участка цепи
Закон Ома для замкнутой цепи и неоднородного участка цепи