Этилацетат этиловый эфир уксусной кислоты. Где применяют этилацетат
Органическая химия зародилась как химия природных соединений, выделенных из организмов животного и растительного происхождения. Заполнение различных классов веществ природными соединениями носит случайный характер и определяется биосинтезом (Карцова А. А. , 2005).
Первая задача органического синтеза – искусственное получение полезных веществ путем копирования природных структур. Этому предшествует стадия выделения природного соединения, изучение его свойств и, наконец, сам органический синтез - воспроизведение в исследовательской лаборатории того, что создано в лаборатории природы. Ну, а затем надо пойти дальше – синтезировать то, что в природе отсутствует.
Ежедневно в мире синтезируется 100 тыс. новых химических соединений, 97 % из которых приходится на долю органических веществ.
Я же решила рассмотреть синтез этилацетата по реакции этерификации.
Этилацетат – это уксусноэтиловый эфир, который находит широкое применение в медицине и ветенарии, в полиграфической промышленности; в качестве растворителя для придания необходимой консистенции краске, отвердителя для закрепления краски, мебельного лака. А также применяется как экстрагент органических соединений из водных растворов, желатинизирующее средство в производстве взрывчатых веществ; входит в состав промышленного термасвариваемого клея. Мировой объем производства этилацетата 0,45-0,5 млн. т в год (1986) (Рид Р. и др. , 1982)
Одним из способов в промышленности этилацетата является этерификация уксусной кислоты этанолом при 110-115° С в присутствии серной кислоты.
Поэтому цель моей работы было проведение синтеза этилацетата по реакции этерификации и изучение его свойства.
Хлористый кальций
Синтез осуществляют в приборе, изображенном на рисунке. В колбу Вюрца емкостью 100мл, снабженную капельной воронкой и соединительную с нисходящим холодильником, вливают 2,5 мл этилового спирта и затем осторожно при перемешивании приливают 1,5 мл концентрированной серной кислоты. Колбу закрывают пробкой, в которую вставлена капельная воронка. И нагревают на масляной (или металлической) бане до 140° С (термометр погружен в баню). В колбу из капельной воронки постепенно приливают смесь из 2 мл этилового спирта и 4,5 мл ледяной уксусной кислоты. Приливание следует вести с такой же скоростью, с какой отгоняется образующий эфир. По окончании реакции (после прекращения отгона эфира) погон переносят в делительную воронку и взбалтывают с концентрированным раствором соды для удаления уксусной кислоты. Отделяют верхний эфирный слой и встряхивают его с насыщенным раствором хлористого кальция (для удаления спирта, который дает с хлористым кальцием кристаллическое молекулярное соединение СаCl2 * C2H5OH, нерастворимое в уксусноэтиловом эфире). Отделив эфир, сушат его прокаленным хлористым кальцием и перегоняют на водяной бане из колбы с дефлегматором. При температуре 71-75° С будет отгоняться смесь спирта и этилацетата, при 75-78° С переходит практически чистый уксусноэтиловый эфир. Выход составляет 20 г (65 % теоретического) (Голодников Г. В. , Мандельштам, 1976).
Результаты
1. Механизм реакции.
В основе получения этилацетата лежит реакция этерификации, в результате которой сложный эфир образуется при нагревании до 140-150 0С уксусной кислоты с этиловым спиртом в присутствии катализатора – серной кислоты.
Общее уравнение реакции
Роль катализатора заключается в протонировании карбонильного кислорода: при этом карбонильный атом углерода становится более положительным и более «уязвимым» по отношению к атаке нуклеофильного агента, которым является молекула спирта. Образующийся вначале катион присоединяет молекулу спирта за счет неподеленных электронов кислородного атома, давая катион:
Катион в результате отщепления протона образует молекулу сложного эфира;
Использование метода «меченых атомов» дало возможность решить вопрос о месте разрыва связей при реакции этерификации. Оказалось, что обычно молекула воды образуется из гидроксила кислоты и водорода спирта. Следовательно, в молекуле кислоты разрывается связь между ацилом и гидроксилом, а в молекуле спирта – связь водорода с кислородом. Такой именно вывод следует из результатов работы по этерификации бензойной кислоты метанолом, содержащим тяжелый изотоп кислорода О18. Полученный сложный эфир содержал в своем составе указанный изотоп кислорода:
Присутствие О18 установлено сжиганием образца эфира и анализом образующихся продуктов сгорании (СО2 и Н2О) на присутствие тяжелого изотопа кислорода (Тюкавкина Н. А. , Бауков Ю. И. , 2004).
Реакция этерификации – обратимый процесс, поэтому во избежание гидролиза полученного продукта, эфир отгоняли с использованием прямого холодильника.
Гидролиз сложных эфиров представляет собой реакцию, обратную реакции их преобразования. Гидролиз может быть осуществлен как в кислой, так и в щелочной среде. Для кислого гидролиза сложных эфиров справедливо все, что было сказано выше применительно к реакции этерификации, об обратимости и механизме процесс, о методах смещения равновесия. Щелочной гидролиз сложных эфиров проходит через следующие стадии:
Практически щелочной гидролиз сложных эфиров проводят в присутствии едких щелочей КОН, NaOH, а также гидроокисей щелочноземельных металлов Ва(ОН)2, Са(ОН)2. Образующиеся при гидролизе кислоты связываются в виде солей соответствующих металлов, поэтому гидроокиси приходится брать по крайней мере в эквивалентном отношении со сложным эфиром. Обычно используют избыток основания. Выделение кислот из их солей осуществляется с помощью сильных минеральных кислот.
При проведении синтеза возможно установление химического равновесия. Согласно принципу Ле-Шателье, чтобы сместить равновесие в сторону образования продукта реакции приливание смеси этилового спирта и ледяной уксусной кислоты проводили с такой же скоростью, с какой отгонялся образующий эфир. Температура синтеза не превышала 150 0С.
При повышении температуры выше указанного значения возможно протекание реакции внутримолекулярной дегидратации:
В результате эксперимента была получена бесцветная с жидкость с характерным запахом. После прекращения выделения эфира полученный продукт переносили в делительную воронку и взбалтывали с концентрированным раствором соды для удаления уксусной кислоты.
Для удаления спирта верхний эфирный слой отделяли и встряхивали его с насыщенным раствором хлористого кальция. Этиловый спирт дает с хлористым кальцием кристаллическое молекулярное соединение состава СаCl2*C2H5OH, нерастворимое в уксусноэтиловом эфире. Отделив эфир, сушили его прокаленным хлористым кальцием.
2. Результаты исследования.
Был рассчитан выход (%) этилацетата в реакции. Согласно закону сохранения массы и энергии теоретический выход эфира составляет 6,3 г (7,0 мл). В результате синтеза было получено 4,5 мл (4,05 г) этилацетата. Выход продукта реакции (этилового эфира уксусной кислоты) равен 64,29 %.
Для идентификации и определения чистоты полученного этилацетата определили угол преломления с помощью рефрактометра. Согласно литературным данным чистый уксусноэтиловый эфир имеет угол преломления, равный 1, 3722. (Рид Р. и др. , 1982). В нашем случае угол преломления этилацетата составил 1,3718 . Данное значение близко к справочным данным, что свидетельствует о достаточной степени чистоты полученного продукта.
Этилацетат (этиловый эфир уксусной кислоты) 88 0,9 1,3722 1,3718 64,29
В результате проведенного синтеза (этерификации уксусной кислоты этиловым спиртом в присутствии серной кислоты при температуре 140 – 150 0С) был получен сложный эфир – этилацетат, который представлял собой прозрачную жидкость с характерным запахом. Для идентификации продукта измерили угол преломления этилацетата (1,3718), который близок к справочным данным. Выход этилового эфира уксусной кислоты составил 64,29%.
Этилацетат (этиловый эфир уксусной кислоты)
Этилацетат (этиловый эфир уксусной кислоты) - бесцветная жидкость с характерным запахом. В литературе указывается, что этилацетат и бутилацетат обладают фруктовым запахом. Возможно. Но большая часть людей, непосредственно работающих с этилацетатом больше склоняются к тому, что его запах напоминает ацетон, чуть с более сладковытым оттенком. Этилацетат - классический представитель сложных эфиров (группа №3 в классификации растворителей для лакокрасочной промышленности. См. раздел «Продукция»).
Эфиры - органические вещества, образующиеся при взаимодействия спиртов и кислот. Спирт+кислота=эфир+вода. (Более подробно См. раздел «Бутилацетат»). Этилацетат - это результат этерификации этилового спирта и уксусной кислоты. Все эфиры практически нерастворимы в воде, но взаимодействуют с водой, вступая в реакцию (гидролиз сложных эфиров -это обратный процесс этерификации).
В результате образуется равновесная система – с одной стороны эфир и вода, с другой спирт и кислота. Хотя этилацетат и не содержит воды, но из-за условий хранения (конденсат в емкостях) или в составе смесевых растворителей, где может присутствовать вода (это растворитель Р-646, Р-645, Р-649, Р-650 т.е практически все растворители в которых есть спирты) этилацетат, взаимодействуя с водой распадается на свои исходные компоненты - уксусную кислоту и зтиловый спирт. Именно поэтому в растворителях в состав которых входят эфиры, со временем повышается кислотность.
Причем этилацетат лучше чем бутилацетат смешивается с водой и более активно с ней взаимодействует. В начале 90-х некоторые талантливые студенты-химики использовали этилацетат для извлечения этилового спирта. Если кто помнит, с алкоголем в магазинах было тяжело, а дешевого этилацетата было много. Этилацетат+вода=этиловый спирт+кислота. Нейтрализуем кислоту и перегоняем полученную смесь. Всем было хорошо.
Этилацетат хорошо смешивается со спиртами, ацетоном, толуолом, ортоксилолом, сольвентом т.е со всеми органическими растворителями. Растворяет эфиры целлюлозы, масла, жиры, хлоркаучуки, виниловые полимеры, карбинольные смолы и т.д. Практически все тоже, что и ацетон, метилацетат, бутилацетат. По растворяющей способности этилацетат близок к ацетону , но слабее его, однако, сильнее бутилацетата . Добавление небольшого количества спиртов – усиливает растворяющую способность этилацетата.
Сырье для производства . Для получения этилацетата применяют техническую уксусную кислоту и этиловый спирт.
Потребление этилацетата. До 90% всего производимого этилацетата потребляет лакокрасочная промышленность (эмали, краски, лаки, грунты, клеи, растворители). Оставшийся объем используется в производстве искуственной кожи, РТИ, пластика и фармацевтики, косметики и пищевой промышленности.
Производители. ОАО «Невинномысский азот» г. Невинномысск Ставропольский край (помимо всего прочего производитель уксусной кислоты и бутилового спирта) входит в состав ОАО Еврохим, ОАО «Ашинский химический завод» Челябинская обл., ОАО «Карбохим» г. Пермь, ОАО «Амзинский лесокомбинат» г. Амзя Башкирия, ФКП «Завод имени Я.М.Свердлова» г. Дзержинск.
Этилацетат ГОСТ 8981-78
| Наименование показателя | Норма по ГОСТ для марки "А" | |
| Высший сорт | Первый сорт | |
| 1. Внешний вид | Прозрачная жидкость без механических примесей | |
| 2. Цветность, единицы Хазена, не более | 5 | 10 |
| 3. Плотность при температуре 20°С, г/см | 0,898-0,900 | 0,897-0,900 |
| 4. Массовая доля основного вещества % не менее | 99,0 | 98,0 |
| 5. Массовая доля кислот в пересчете на уксусную кислоту, %, не более | 0,004 | 0,008 |
| 6. Массовая доля нелетучего остатка, %, не более | 0,001 | 0,003 |
| 7. Температурные пределы перегонки при давлении 101,3 кПа(760 мм рт.ст.): 95% (по объему) продукта должно отгоняться в пределах температур, С° | 75 - 78 | 74 - 79 |
| 8. Массовая доля воды, %, не более | 0,1 | 0,2 |
| 9. Массовая доля альдегидов в пересчету на уксусный альдегид, %, не более | не более 0,05% | Не нормируется |
| 10. Относительная летучесть (по этиловому эфиру) | 2 - 3 | 2 - 3 |
Этилацетат (Этиловый эфир уксусной кислоты) можете купить на нашем складе, рядом с г. Подольск и г. Климовск
Хорошо растворяется в спирте, хлороформе и эфире, в воде растворяется хуже, хорошо горит, предельная взрывоопасность имеет концентрацию в воздухе 2,2 - 9%. Это растворитель, имеющий небольшую стоимость, малую токсичность, обладающий приемлемым запахом.
Этилацетат получается при:
Ацетилировании этилового спирта хлористым ацетилом или уксусным ангидридом. (Лабораторный способ)
. перегонке смеси этилового спирта, уксусной и серной кислот. (Промышленный способ).
. обработке этилового спирта кетеном. (Промышленный способ).
. по реакции Тищенко из ацетальдегида при 0-5 °C в присутствии каталитических количеств алкоголята алюминия. (Промышленный способ)
Технические характеристики этилацетата .
Наименование показателей | Норма |
| Внешний вид этилацетата | бесцветная, прозрачная жидкость, не содержащая механических примесей |
| Плотность этилацетата при 20 °С, г/см*3 | 0,898-0,900 |
| Цветность единицы Хазена | 5 |
| Массовая доля основного вещества, %, не менее | 99,0 |
| Массовая доля уксусной кислоты, %, не более | 0,004 |
| Массовая доля нелетучего остатка, %, не более | 0,001 |
| Температурные пределы перегонки этилацетата при давлении 760 мм. рт. ст., °С | 75-78 |
| Массовая доля воды, %, не более | 0,1 |
| Относительная летучесть (по этиловому эфиру) | 2-3 |
| Массовая доля этилового спирта | отсутствует |
Характеристика этилацетата по маркам и сортам.
| Наименование показателя | Этилацетат | ||
| А | Б | ||
| высший сорт | 1-й сорт | ||
| Внешний вид | Прозрачная жидкость без механических примесей | ||
| Цветность, единицы Халена, не более | 5 | 10 | 10 |
| Плотность при 20 0С, г/см3 | 0,898-0,900 | 0,897-0,900 | 0,890-0,900 |
| Массовая доля основного вещества, % | не менее 99 | не менее 98 | 91±1 |
| Массовая доля кислот в пересчете на уксусную кислоту, %, не более | 0,004 | 0,008 | 0,01 |
| Массовая доля нелетучего остатка, % , не более | 0,001 | 0,003 | 0,007 |
| Температурные пределы перегонки при давлении 101,3 кПа 93% (по объему) продукта должны отгоняться в пределах температур, 0С | 75-78 | 74-79 | 70-80 |
| Массовая доля воды, % не более | 0,1 | 0,2 | 1 |
| Массовая доля альдегидов в перерасчете на уксусный альдегид, % не более | 0,05 | не маркируется | - |
Этилацетата используется в следующих отраслях промышленности:
Как растворитель в производстве лакокрасочных материалов и чернил для печатающих машин;
. как растворитель в изготовлении клеевых композиций;
. на стадии упаковывания различных товаров гибкими упаковочными материалами - как растворитель чернил при нанесении надписей и изображений трафаретным способом;
. как реагент и как реакционная среда в производстве фармацевтических препаратов (метоксазол, рифампицин и т.д.);
. как обезжиривающий агент в производстве алюминиевой фольги и тонких алюминиевых листов;
. как очищающий и обезжиривающий агент в электронной промышленности;
. как растворитель эфиров целлюлозы;
. в смеси со спиртом как растворитель в производстве искусственной кожи;
. как экстрагирующий агент для различных органических веществ из водных растворов. Благодаря низкой токсичности этилацетат используется в пищевой промышленности, например, для экстрагирования кофеина из кофе.
. как желатинизирующее средство при изготовлении взрывчатых веществ;
. как компонент фруктовых эссенций;
Структурная формула
Истинная, эмпирическая, или брутто-формула: C 4 H 8 O 2
Молекулярная масса: 88,106
Этилацетат - (этиловый эфир уксусной кислоты) СН 3 -СОО-CH 2 -CH 3 - бесцветная летучая жидкость с резким запахом.
Получение
Этилацетат образуется при прямом взаимодействии этанола с уксусной кислотой :
CH 3 COOH + C 2 H 5 OH → CH 3 COOC 2 H 5 + H 2 O
Лабораторный метод получения этилацетата заключается в ацетилировании этилового спирта хлористым ацетилом или уксусным ангидридом :
CH 3 COCl + C 2 H 5 OH → CH 3 COOC 2 H 5 + HCl
К промышленным способам синтеза этилацетата относятся:
Перегонка смеси этилового спирта , уксусной и серной кислот.
Обработке этилового спирта кетеном.
По реакции Тищенко из ацетальдегида при 0-5 °C в присутствии каталитических количеств алкоголята алюминия:
2CH 3 CHO → CH 3 COOC 2 H 5
Физические свойства
Бесцветная подвижная жидкость с резким запахом эфира. Молярная масса 88,11 г/моль, температура плавления −83,6 °C, температура кипения 77,1 °C, плотность 0,9001 г/см³, n204 1,3724. Растворяется в воде 12 % (по массе), в этаноле , диэтиловом эфире , бензоле , хлороформе ; образует двойные азеотропные смеси с водой (т. кип. 70,4 °C, содержание воды 8,2 % по массе), этанолом (71,8; 30,8), метанолом (62,25; 44,0), изопропанолом (75,3; 21,0), CCl4 (74,7; 57), циклогексаном (72,8; 54,0) и тройную азеотропную смесь Э.: вода : этанол (т. кип. 70,3 °C, содержание соотв. 83,2, 7,8 и 9 % по массе).
Применение
Этилацетат широко используется как , из-за низкой стоимости и малой токсичности, а также приемлемого запаха. В частности, как нитратов целлюлозы, ацетилцеллюлозы, жиров, восков, для чистки печатных плат, в смеси со спиртом - в производстве искусственной кожи. Годовое мировое производство в 1986 году составляло 450-500 тысяч тонн. Мировое производство этилацетата на 2014 год составляет около 3,5 млн. тонн в год.
Один из самых популярных ядов, применяемых в энтомологических морилках для умерщвления насекомых. Насекомые после умерщвления в его парах гораздо мягче и податливее в препарировании, чем после умерщвления в парах хлороформа.
Применяется как компонент фруктовых эссенций. Зарегистрирован в качестве пищевой добавки E1504.
Лабораторное применение
Этилацетат часто используется для экстракции, а также для колоночной и тонкослойной хроматографии. Редко в качестве для проведения реакций из-за склонности к гидролизу и переэтерефикации.
Используется для получения ацетоуксусного эфира:
2CH 3 COOC 2 H 5 → CH 3 COCH 2 COOC 2 H 5
Очистка и сушка
Продаваемый этилацетат обычно содержит воду , спирт и уксусную кислоту . Для удаления этих примесей его промывают равным объёмом 5%-го карбоната натрия , сушат хлоридом кальция и перегоняют. При более высоких требованиях к содержанию воды несколько раз (порциями) добавляют фосфорный ангидрид, фильтруют и перегоняют, защищая от влаги. С помощью молекулярного сита 4А содержание воды в этилацетате можно снизить до 0,003 %.
Безопасность
ЛД 50 для крыс составляет 11,6 г/кг, показывая низкую токсичность. Пары этилацетата раздражают слизистые оболочки глаз и дыхательных путей, при действии на кожу вызывают дерматиты и экземы. ПДК в воздухе рабочей зоны 200 мг/м³. ПДК в атмосферном воздухе населенных мест 0,1 мг/м³. Температура вспышки - 2 °C, температура самовоспламенения - 400 °C, концентрационные пределы взрыва паров в воздухе 2,1-16,8 % (по объему). Безопасность при транспортировке. В соответствии с ДОПОГ (ADR) класс опасности 3, код по реестру ООН 1253.
представляет собой бесцветную летучую жидкость с приятным фруктовым запахом. Растворяется в этаноле, диэтиловом эфире, бензоле, хлороформе, толуоле и ряде других органических растворителях. В воде растворяется хуже (до 12% по массе), хорошо горит. Обладает всеми свойствами сложных эфиров, является умеренно полярным растворителем. Хорошо растворяет эфиры целлюлозы, смоляные масляные лаки, жиры, воски.Плотность - 0,902 г/см³. Температура плавления -83° C, температура кипения 77° C.
Этилацетат получают промышленным способом методом перегонки смеси этилового спирта, уксусной и серной кислот, а также методом обработки этилового спирта кетеном, или по реакции Тищенко из ацетальдегида при 0-5° C в присутствии каталитических количеств алкоголята алюминия.
Химическая формула: C 4 H 8 O 2 .
Применение этилацетата.
Как растворитель, являясь активным растворителем нитро- и этилцеллюлозы, широко используется в производстве лакокрасочных материалов и чернил для печатающих машин. Также он входит в композиции растворителей нитроглифталевих, перхлорвиниловых и эпоксидних эмалей, разных смазочных масел, восков, полиэфирных лаков, красок, кремниорганических лаков и эмалей. На эти цели расходуется до 30% всего производимого этилацетата;
Как растворитель в изготовлении клеевых композиций;
На стадии упаковывания различных товаров гибкими упаковочными материалами - как растворитель пленок и чернил при нанесении надписей и изображений трафаретным способом;
Как реагент и как реакционная среда в производстве фармацевтических препаратов (метоксазол, гидрокортизон, рифампицин и т.д.);
Как обезжиривающий агент в производстве алюминиевой фольги и тонких алюминиевых листов;
Как очищающий и обезжиривающий агент в электронной промышленности;
В производстве кино- и фотопленки, целлофана, различных резино-технических изделий;
В смеси со спиртом как растворитель в производстве искусственной кожи;
Как экстрагирующий агент для различных органических веществ из водных растворов. Благодаря низкой токсичности этилацетат используется в пищевой промышленности, например, для экстрагирования кофеина из кофе;
Как желатинизирующее средство при изготовлении взрывчатых веществ;
Как компонент (пищевая добавка E1504) фруктовой эссенции, которую добавляют в прохладительные напитки, ликеры и кондитерские изделия.
| Наименование показателя | Норма для марки и сорта | ||
| Марка А | Марка Б | ||
| Высший сорт | Первый сорт | ||
| Внешний вид | Прозрачная жидкость без механических примесей | ||
| Цветность по платиново-кобальтовой шкале, ед. Хазена, не более | 5 | 10 | 10 |
| Плотность при 20° С, г/см³ | 0,898-0,900 | 0,897-0,900 | 0,890-0,900 |
| Массовая доля этилацетата, % | не менее 99,0 | не менее 98,0 | 91,0±1 |
| Массовая доля кислот в пересчете на уксусную кислоту, %, не более | 0,004 | 0,008 | 0,010 |
| Массовая доля нелетучего остатка, %, не более | 0,001 | 0,003 | 0,007 |
| Температурные пределы перегонки при давлении 101,3 кПа (760 мм рт.ст.): 95% (по объему) продукта должно отгоняться в пределах температур, ° С |
75-78 |
74-79 |
70-80 |
| Массовая доля воды, %, не более | 0,1 | 0,2 | 1,0 |
| Массовая доля альдегидов в пересчете на уксусный альдегид, %, не более | 0,05 | не нормируется | - |
| Относительная летучесть (по этиловому эфиру) | 2-3 | 2-3 | 2-3 |
Требования безопасности.
Этилацетат технический по степени воздействия на организм человека относится к числу малоопасных веществ (4 класс опасности). Пары этилацетата раздражают слизистые оболочки глаз и дыхательных путей. При действии на кожу вызывают дерматиты и экземы. ПДК в воздухе рабочей зоны 200 мг/м⊃3.
Этилацетат технический является легковоспламеняющейся жидкостью и образует в смеси с воздухом взрывоопасную смесь категории ПА, группы Т2 по ГОСТ 12.1.011.
 Ударение в английском языке
Ударение в английском языке 10 слов с ударением на 1 слог
10 слов с ударением на 1 слог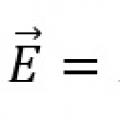 Закон Ома для замкнутой цепи и неоднородного участка цепи
Закон Ома для замкнутой цепи и неоднородного участка цепи